HOME > 口腔感染症を理解するために
口腔感染症を理解するために
口腔感染症の意味論
「常在菌と共生できる期間を寿命」という。それを最も良く現しているのが口腔感染症で、これらの視点から口腔内細菌、口腔感染症、そして口腔感染症を誘因とする全身疾患を見ると常在菌と生体との関係が良く理解できる。その背景として知っておくことは①口腔感染症は常在細菌による内因性の感染症で、主な原因は宿主側にあること。②生体防御能の主役である免疫担当細胞は、血液により口腔組織内を含む体内を循環する。そして、③口腔は消化器官の一部であり、健康と免疫機能維持に重要な食物は全て口腔から摂取されることである。多くの研究から、細菌学的にも、免疫学的にも、「口腔の情報は全身に伝わり、全身の情報は口腔に伝わる」ことが証明されている。つまり、口腔の健康状態は全身の健康状態と免疫年齢を如実に表していることを意味している。常在菌とのより良い共生関係を維持し、健康に寿命を全うするために、医歯連携による口腔ケアが一層重要となる。
う蝕と歯周病に代表される口腔感染症は、国民の大部分が罹患する感染症であるにもかかわらず、一般には生活習慣病と考えられている。また、直接生命に関わる感染症でないという認識も強い。近年の基礎研究や疫学調査により、歯周病などの口腔感染症が糖尿病や動脈硬化、自己免疫疾患、心臓血管障害、腎臓病や肥満などさまざまな全身疾患の誘因となることが明らかになってきた。また、直面している臨床上の大きな問題としては、直接の死因となる口腔内細菌による誤嚥性肺炎、さらに、がん治療患者の口腔内疾患と緩和ケアがある。このように、口腔の感染症はさまざまな形で全身に大きな影響を与えているといえる。
急性期病院における口腔ケアは、主に患者のQOL(Quality of Life)の向上を中心に考えられてきたが、患者の在院日数の短縮や使用薬剤の削減など医療経済的にも大きな効果があることが数多く報告されている。しかし、現時点において医科、歯科および看護における口腔ケアに対する認識の差は大きく、意思統一がなされているとはいい難い。より一層の医歯連携の医療を推進するためには、より多くの科学的根拠が必要となる。そこで、われわれの講座においては、研究面における緊密な医歯連携を実現し、新たな視点から口腔疾患と難治性全身疾患の関連性を見直しEvidenced Based Medicineに貢献することを目的としている。
口腔感染症とは
口腔は、消化器官の一部として外界に接すると共に、粘膜面から歯という硬組織が植立している特殊な器官といえる。したがって、歯と粘膜上皮という異なった部位にそれぞれ特徴ある細菌叢が形成される。口腔感染症を理解するためには、以下の内容を良く理解する必要がある。
1.口腔感染症は内因性混合感染症である。
口腔内には、未同定の細菌を含め、約700種類の細菌が生息している。出生直後から母親や近親者から伝搬した細菌が歯面や粘膜面に付着し、複雑なバイオフィルムを形成するため外来性の細菌が付着増殖することは困難である。したがって、口腔の感染症の多くは、口腔内常在菌が原因である。また、個々の細菌は病原性が弱いため、単独で疾患を起こすのではなく混合感染の様式をとる。歯周病はその代表的疾患といえる。また、一般に慢性感染症として推移する。
2.口腔内からは強病原性菌は検出されない。
先に記載したように、口腔細菌叢形成菌の病原性は極めて弱い。また、代表的歯周病原菌Porphyromonas gingivalisの内毒素の生物活性は、大腸菌などの一般細菌に比べ、極めて低い。したがって、う蝕や歯周病などの口腔疾患に見られるように、発症までに長時間を要する。
3.口腔フローラ形成菌の特徴;
- 1)歯や口腔粘膜に付着する菌だけが口腔内に定着できる。
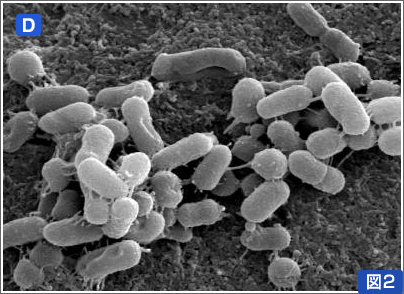
- 2)主な生息部位はデンタルプラークで、典型的なバイオフィルムを形成する。さらに、歯肉縁上と縁下プラークとでは菌叢が異なり、前者では通性嫌気性グラム陽性レンサ球菌が中心に、グラム陽性桿菌が共存する(図1)。一方、縁下プラークからは、通性嫌気性グラム陽性レンサ球菌や桿菌が検出されるものの、偏性嫌気性グラム陰性桿菌も生息する。
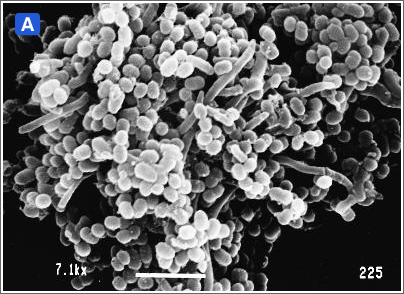
- 3)プラーク形成菌は凝集性が強く、単一菌種の凝集だけではなく、異菌種間凝集が見られる。凝集菌塊は抗食菌性、耐酸性などを示すため、一部の細菌は糞便からも培養される(図2)。
4.初期プラーク形成菌は口腔環境維持に重要である。
主にレンサ球菌により形成される初期プラークは、外来性の細菌の口腔内定着を阻害する。健康的な口腔の維持には、レンサ球菌中心の細菌叢を保つことが重要である。
5.プラークの増加に伴い病原性プラークへ遷移する。
不十分な口腔ケアにより経時的にプラーク量が増加する。歯や粘膜面に直接付着出来ない菌も、異菌種間の凝集により初期プラーク形成菌に付着することで定着が可能となる。その結果、フラーク量は飛躍的に増加し、菌叢も複雑な様相を呈してくる。また、プラーク量の増加と共にプラーク深部の酸化還元電位が低下し、偏性嫌気性菌の発育が可能となる。偏性嫌気性グラム陰性桿菌比率が増加するにしたがって、歯肉の炎症や歯周病が発症しやすい環境となる(図3)。
6.発症には宿主の生体防御能の低下が重要である。
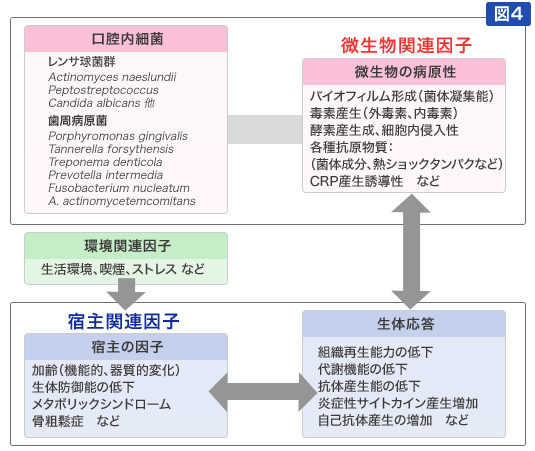
口腔は外界と直接接触するため、さまざまな生体防御能が発達している強固な器官である。しかし、加齢変化や種々の基礎疾患により宿主の防御能が低下するにしたがって口腔感染の発症率は増加する。一般的に口腔感染症は発症までにさまざまな因子が関わり時間を要するため、一部に生活習慣病との認識がなされているが、う蝕や歯周病は細菌感染症である。ただし、細菌の関与は必須であるものの、宿主の生体防御能の変化も重要な因子といえる(図4)。
図1:デンタルプラーク
口腔細菌の主な生息部位であるプラークは典型的なバイオフィルムで、歯肉縁上および歯肉縁下プラークに分けられる。歯肉縁上プラークは歯面に形成されるもので、主にレンサ球菌を中心とした通性嫌気性グラム陽性菌を中心に構成される。歯肉縁下プラークは、やや複雑であるものの、類似の細菌が検出される。しかし、プラーク量の増加と共に歯肉縁下プラークでは偏性嫌気性グラム陰性桿菌の比率が増し、歯周炎などの原因となる。
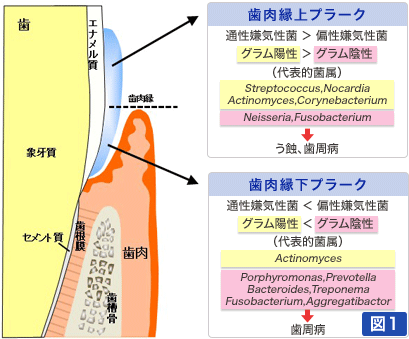
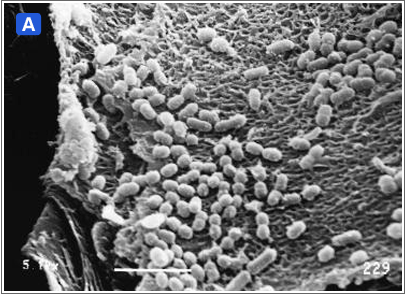
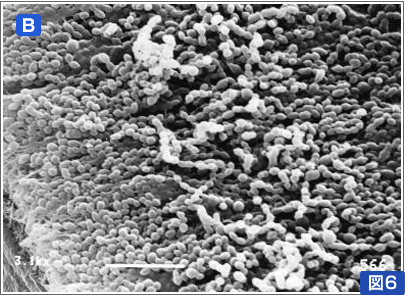
図2:歯肉縁下プラークにおける細菌叢の遷移(走査電子顕微鏡写真)
健常者の歯肉縁下プラークは主にグラム陽性球菌と桿菌が検出される(A)。慢性歯周炎患者の歯肉ポケットに形成されるプラークでは、グラム陰性嫌気性桿菌が増加し細菌叢に遷移がおこり、より複雑なプラークが形成され病原性プラークとなる(B)。多くの赤血球も観察される。また、糸状菌上に球菌や小桿菌が異菌種間で共凝集し形成される穂軸状構造物 corn-cob(C、矢印)やT. denticolaなどのスピロヘータが多数認められる(C)。代表的な歯周病原細菌Porphyromonas gingivalis(D)。本菌の内毒素(LPS)、プロテアーゼ、線毛、酪酸などが病原因子となり歯肉や歯槽骨の破壊がおこる(歯周病)。近年、歯周病が糖尿病などの全身疾患の発症に関わっていることが明らかとなってきた。
図3:デンタルプラーク内における異菌種間凝集
初期定着細菌群が歯面上に形成された唾液ペリクル(獲得皮膜)に特異的に吸着し、初期プラークを形成する。その後、異菌種間凝集などにより直接歯面に付着する能力のない後期定着菌群が蓄積し、細菌叢に遷移が起こり病原性プラークが形成される。(文献1を引用改変)
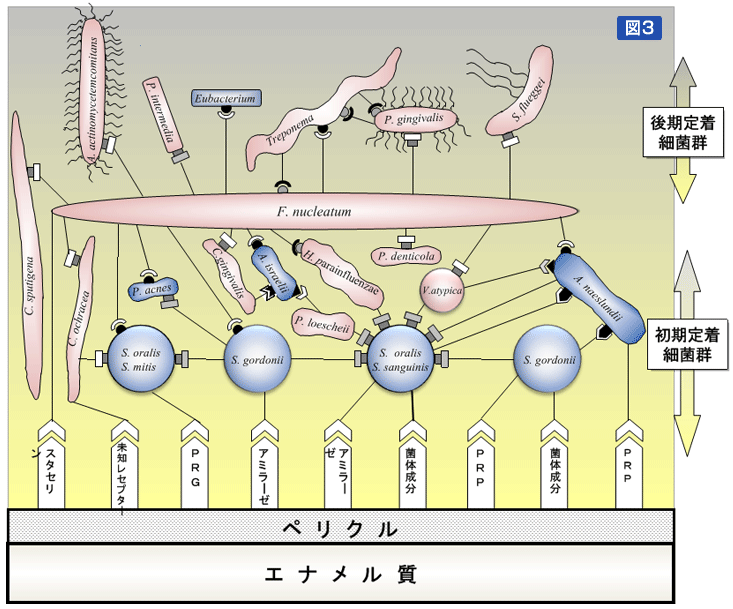
図4:口腔感染症の発症に関連する因子
![]()
- 1)Richard AH, et al: Bacterial coaggregation: an integral process in the development of multi-species biofilm. Trends Microbiol 11: 94-100, 2003
- 2)奥田克爾:口腔内バイオフィルム、医歯薬出版、東京、2004
- 3)Rose LF et al ed : "Periodontal medicine" BC Decker Inc. London, Saint Louis, 2000 (宮田 隆監訳、:ペリオドンタルメディスン、医歯薬出版、東京2001
- 4)下野正基ほか:歯周病の病態、 "Preventive periodontology" 鴨井久一、花田信弘、佐藤勉、野村義昭偏、医歯薬出版、東京、p.8-22、2007
- 5)落合邦康: 序 口腔感染症の意味論-口腔内細菌による全身疾患と口腔ケア-. 化学療法の領域, 27(1) 18-21
口腔感染症をより理解するために
1.全身免疫状態が反映する口腔粘膜
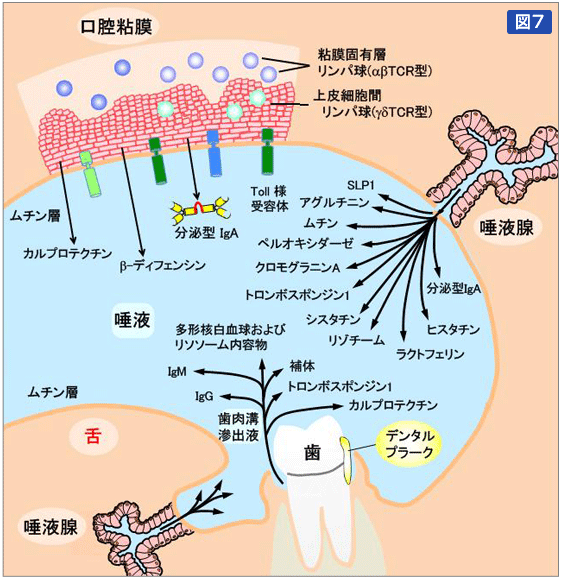
口腔には、未同定の細菌を含め約700種、腸内フローラに匹敵するほど多種類の常在細菌が生息している。その主な生息部位は、歯肉縁上・縁下に形成されるオーラバイオフィルム、つまりデンタルプラーク(以下プラーク)で、その細菌密度は糞便のそれよりはるかに高い(図5)。管理下にあるプラークは、口腔環境の維持に働き宿主とは良好な共生関係が保たれる。しかし、不十分なケアによるプラーク量の増加は、う蝕そして加齢や生体防御能の低下などの因子が加わると"慢性炎症性疾患・歯周病"などの口腔疾患が発症する。口腔感染症は典型的な内因性混合感染症で、慢性症状を示すため生体と共生細菌との相互作用を研究する上で極めて興味あるモデルといえる。つまり、腸内フローラの主な共生部位である大腸は、厚いムチン層で覆われるため粘膜上皮と腸内細菌が直接触れる機会は少ない。しかし、口腔では唾液成分ムチンからなる厚さ0.1~0.2μmのペリクル(獲得被膜)を介して細菌が直接粘膜や歯に付着する(図6)。口腔内で細菌抗原により感作されたリンパ球は末梢血からも検出される。また、腸管粘膜を口腔細菌で刺激すると、感作されたリンパ球は帰巣循環経路により口腔粘膜下に移動し、抗体を産生する。その結果、唾液腺からは抗原特異的な分泌型IgA抗体が、そして歯肉溝液からはIgGが検出される(図7)。この現象は「口腔の情報は全身に伝わり、全身の情報が口腔に伝わる」ことを示している。常に細菌接触により刺激を受ける口腔粘膜上皮細胞は、さまざまな抗菌因子を活発に産生し細菌の排除を行う一方で、炎症性サイトカインの産生を抑制して粘膜の炎症を防いでいる。口腔粘膜では、常に細菌が侵入し軽度の炎症が起る可能性があるためにこのような仕組みが発達した可能性がある。つまり、口腔感染症の発症は全身免疫能の低下そのものを意味している。
2.口腔細菌の特徴と病原性
口腔内には1日約1,000 ~ 1,500 mLもの唾液が分泌される。唾液には抗体やさまざまな抗菌物質が含まれ菌の発育を抑制しているが、IgAプロテアーゼを産生するなどこれらの因子に抵抗し、口腔粘膜や歯に付着できる菌のみが口腔フローラを形成する。唾液1mL中には約10の8乗~9乗個もの細菌が存在するが、義歯装着者の唾液からはさらに多くの細菌が検出される。歯頚部や歯の隣接面などには過剰のプラークが形成され成熟プラークとなり、1g中には約10の10乗~11乗個の細菌が存在する。口腔フローラからは強い病原性を持つ細菌は全く検出されないが、これらの細菌が誤嚥性肺炎などの原因となる。
3.全身疾患発症の意味
プラーク形成菌や口腔感染症病巣が原因となる全身疾患は、細菌が主因というよりは、加齢による宿主の器質的、機能的障害や患者の生体防御能の低下など宿主側の因子が主な原因と考えられる。これを明確に示す現象が、がんの化学療法、放射線療法時に発症するさまざまな口腔疾患や感染症である。薬物療法や放射線療法により口腔粘膜の潰瘍や口腔乾燥症が発症し、さらに免疫力の低下が認められる。その結果、口腔内常在細菌やウイルスによりカンジダ症、重症の歯周疾患、そして口腔ヘルペスなどの感染症が頻症する。しかし、これらの患者においても、口腔ケアにより口腔内の細菌数を減少させることにより、確実に組織の炎症が改善し症状は緩和される。つまり、全身の免疫状態と常在細菌相互の力関係が明確に認識できる器官、それが口腔である。
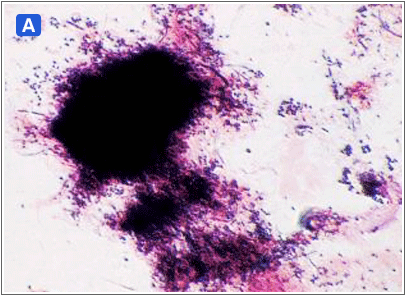
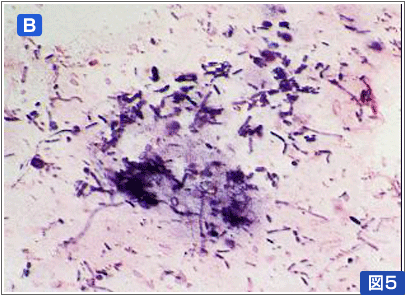
図5:デンタルプラークと糞便の比較(グラム染色)
歯肉縁上プラーク(A)は形成菌主にレンサ球菌を中心構成されるが、腸内フローラ形成菌(B)と異なり、常に凝集塊を形成するため細菌密度が高い。
図6: 口腔粘膜に付着した口腔細菌
(A)。全ての口腔粘膜に細菌が付着している。ウシエナメル質ブロックを義歯床に装着し、口腔内にて2日経過後にエナメル質上に形成されたプラーク(B)。一面にレンサ球菌を中心としたバイオフィルムが形成されている。
図7: 口腔の感染防御機構
口腔内には、唾液腺や歯肉溝および粘膜上皮からさまざまな抗菌物質が分泌されている。特に唾液の役割は重要で、さまざまな自浄作用の中心的役割を果たしている。また、粘膜上皮細胞は、Toll-like受容体(TLR)などを発現し自然免疫に関与すると共に、細菌刺激により抗菌物質の産生が促進される。